Biotekselskabet Acesion Pharmas vej mod en kur for atrieflimren
Af Luca Soattin
ARSID interviewer prof Bo Hjorth Bentzen hos Acesion Pharma
I 1623 gav den engelske læge W. Harvey, elev af G. Galilei, den første formelle beskrivelse af hjertets bevægelser. Dette førte til kinematisk medicin: præcedit motus auricularum et subsequit cordis, et motus ab auriculis incipere, et in ventriculos progredi visus est (bevægelsen af atrierne sker først, efterfulgt af bevægelsen af resten af hjertet). Det ser ud til, at bevægelsen begynder fra atrierne og breder sig til ventriklerne). Hjertet består overordnet set af to atrier, der opsamler blodet, og to ventrikler, hvoraf det ene pumper blodet kraftigt ud til organerne, mens det andet fører det iltfattige blod til lungerne. Denne fascinerende tidsmæssige synkronisering af hjertets sammentrækning skyldes elektriske impulser, der automatisk genereres i en lille del af hjertet kaldet sinusknuden. Tiden det tager for den nodale elektriske impuls at sprede sig i hele hjertet medfører, at atrierne kontraherer før ventriklerne, hvormed blodet overføres koordineret mellem hjertets kamre. Dette komplekse system af elektrisk ledning reguleres nøje af ionkanaler i hjertecellerne, som, når den elektriske impuls passerer, tillader strømmen af ioner (natrium, calcium og kalium) over cellemembranen, hvilket muliggør kontraktion. Hvad sker der, hvis denne raffinerede kombination af bioelektriske begivenheder bliver kompromitteret? Forestil dig at danse, hvor du nøje følger bestemte trin. Hvis du tager fejl af et trin, skal du komme tilbage, og mens du gør det, vil du være ude af trit, hvilket skaber en arytmi. Hjertearytmier er talrige og udgør en ekstremt heterogen gruppe. Hvis der opstår ændringer i rytmen, kan hjertet muligvis ikke fyldes tilstrækkeligt, så det ikke længere kan udføre pumpefunktionen korrekt.
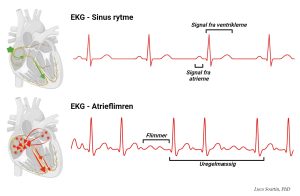 Atrieflimren (AF) er den mest udbredte arytmi i Europa og i verden. Det European Society of Cardiology har anslået, at der i 2060 vil være mere end 14 millioner mennesker i Europa med AF. Det præcise rytmiske apparat, som regulerer hjertets elektriske ledning, fungerer ikke længere korrekt for AF patienter. Elektriske impulser vil afgå fra forskellige steder i atrierne, resulterende i en kaotisk signalering og en stigning i hjertefrekvensen. Over tid udvikler dette sig til en kronisk tilstand, der fører til udvidelse af atrierne, blodstagnation og dannelse af blodpropper, som, når de når den venstre ventrikel, kan frigives i blodbanen og forårsage blodpropper i bl.a. hjernen.
Atrieflimren (AF) er den mest udbredte arytmi i Europa og i verden. Det European Society of Cardiology har anslået, at der i 2060 vil være mere end 14 millioner mennesker i Europa med AF. Det præcise rytmiske apparat, som regulerer hjertets elektriske ledning, fungerer ikke længere korrekt for AF patienter. Elektriske impulser vil afgå fra forskellige steder i atrierne, resulterende i en kaotisk signalering og en stigning i hjertefrekvensen. Over tid udvikler dette sig til en kronisk tilstand, der fører til udvidelse af atrierne, blodstagnation og dannelse af blodpropper, som, når de når den venstre ventrikel, kan frigives i blodbanen og forårsage blodpropper i bl.a. hjernen.
AF er faktisk ansvarlig for over 20% af slagtilfælde og er en stor belastning for nationale sundhedssystemer. I dag er den primære behandling interventionsradiologi. Ved at nå hjertet med bestemte elektroder foretages elektrisk isolering af de områder, der genererer disse aritmetiske hændelser. Men det er ikke altid løsningen. Forskningsindsatsen går ud på at identificere nye farmakologiske mål for udvikling af skræddersyede lægemidler. Vi har i dag fornøjelsen af at snakke med prof Bo H. Bentzen, medstifter af Acesion Pharma, en dansk bioteknologivirksomhed, der siden 2011 har haft til formål at udvikle effektive lægemidler til behandling af AF. I september sidste år modtog Acesion Pharma en finansiering på 336 mio. kr. til at starte kliniske forsøg med AP31969, et oralt lægemiddel mod AF.
Kan du forklare, hvorfor der stadig ikke findes effektive lægemidler mod AF, og hvilke begrænsninger de nuværende terapier har?
Historisk set har det vist sig vanskeligt at udvikle lægemidler, som kan modvirke AF uden samtidig at øge risikoen for, at der opstår arytmier i hjertets ventrikler. Det skyldes bl.a. at hidtidige lægemidler virker ved at hæmme ionkanaler, som både findes i hjertets ventrikler og atrier. Det er netop den uhensigtsmæssige farmakologiske hæmning af ionkanaler i ventriklerne, der øger risikoen for udvikling af farlige bivirkninger i form af ventrikulære hjertearytmier i udsatte patienter.
 Hvad er SK-kanaler, og hvorfor er de så vigtige i AF?
Hvad er SK-kanaler, og hvorfor er de så vigtige i AF?
SK-kanaler er en gruppe af ionkanaler, som tillader at kalium kan løbe ud af hjertecellerne, når mængden af calcium stiger. Grunden til vi er så fascineret af SK-kanaler er, at de primært findes i atrier og ikke ventrikler, og vi har vist, at man ved hjælp af nye lægemiddelkandidater, som hæmmer SK-kanalen, kan standse AF uden at hjertets ventrikler påvirkes. Dermed forventer vi, at lægemidler, som hæmmer SK-kanalen, ikke vil have den samme bivirkningsprofil med øget risiko for ventrikulære arytmier, som andre lægemidler og lægemiddelkandidater har haft. Genetisk set har SK-kanalen også en særlig rolle i AF. Internationale genetiske studier med hundredtusindvis af deltagere har vist, at SK-kanalen er associeret med udviklingen af AF. Vi har således både en mekanistisk og genetisk forståelse og håb om, at SK-kanalen er et godt angrebspunkt for udvikling af ny medicin til behandling af AF.
Hvordan opstod AP31969, og hvordan fungerer det?
AP31969 opstod som følge af mange års forskning og afprøvning. Vores medicinal kemikere har arbejdet hårdt på at udvikle den bedste lægemiddelkandidat til behandling af AF. AP31969 hæmmer selektivt SK-kanalen, og fokus har især været på at minimere risikoen for ventrikulære bivirkninger.
 Generelt viser statistikken, at ét lægemiddel ud af ti tusind når de sidste faser af kliniske forsøg. Det er en meget lille andel, og det repræsenterer en betydelig iværksætterrisiko. Hvad er de største udfordringer ved at udvikle et lægemiddel mod AF?
Generelt viser statistikken, at ét lægemiddel ud af ti tusind når de sidste faser af kliniske forsøg. Det er en meget lille andel, og det repræsenterer en betydelig iværksætterrisiko. Hvad er de største udfordringer ved at udvikle et lægemiddel mod AF?
De største risici ved udvikling af ny medicin til behandling af AF er at udvikle et lægemiddel, som er sikkert og effektivt. Som sagt tidligere, så har et stort problem for udviklingen af nye
lægemidler til behandling af AF været, at de viser sig at øge risikoen for ventrikulære bivirkninger.
Der er mange investorer og store medicinalfirmaer, der har brændt fingrene på dette. Vores tilgang er anderledes end, hvad der hidtil har været forsøgt, og vi har stærke forskningsresultater og resultater fra kliniske forsøg, som indikerer at SK-kanalen udgør et meget attraktivt angrebspunkt for behandling af AF.
Vi takker Peter Raabye og Emma H. Meibom for at have gennemgået teksten











